Fluides supercritiques : liquides et gazeux… en même temps
Dans cet état entre liquide et gaz, les corps acquièrent des propriétés surprenantes, très utilisées dans l'industrie chimique pour remplacer les solvants organiques nocifs.
Cet article est issu du magazine Les Indispensables de Sciences et Avenir n°210 daté juillet/ septembre 2022.
Boire un café décaféiné, se délecter d'un parfum, déguster un vin sans goût de bouchon… Ces moments de plaisir n'existeraient pas sans les surprenants fluides dits "supercritiques". Pour comprendre ce qu'est l'état supercritique de la matière, le plus simple est d'observer le diagramme de phase d'une substance chimique pure, qui décrit l'état de celle-ci - liquide, solide ou gazeux -en fonction de la température et de la pression ambiantes.
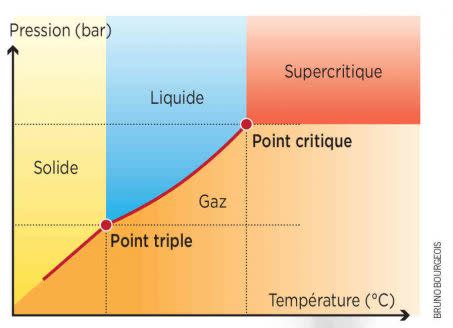
Diagramme de phase d'une substance chimique pure, qui décrit l'état de celle-ci - liquide, solide, gazeux ou... les deux - en fonction de la température et de la pression ambiantes. Crédit : Bruno Bourgeois
En faisant augmenter ces deux paramètres, on atteint un "point critique" au-delà duquel la frontière entre liquide et gaz finit par s'effacer. "On dit alors du corps qu'il est supercritique. Il présente à la fois les propriétés d'un liquide et celles d'un gaz", explique Stéphane Sarrade, chercheur en génie des procédés et directeur des programmes Énergie au CEA. Dense comme un liquide, mais faiblement visqueux, il s'écoule aisément et peut aussi diffuser comme un gaz, dans un milieu poreux par exemple. Une aubaine pour l'industrie chimique, qui l'utilise dans de nombreuses applications.
"Le CO2 supercritique a intéressé très tôt les chimistes"
La plus ancienne est celle du CO2 supercritique, dont le point critique, à 31°C et 73 bars de pression, peut être aisément atteint. "Le CO2 supercritique a intéressé très tôt les chimistes, car il a un pouvoir solvant : à partir d'un mélange de molécules, il permet d'isoler celle qui nous intéresse. C'est notamment le cas de la caféine du café", souligne Stéphane Sarrade. Jusqu'aux années 1970, la production de café décaféiné s'effectuait à l'aide de solvants organiques tels que le trichloréthylène ou le chloroforme. Problème : leurs résidus sont toxiques pour l'organisme. Les i[...]
Lire la suite sur sciencesetavenir.fr

 Yahoo Actualités
Yahoo Actualités 